유전자 변이가 예후를 결정합니다 – 선천성·영아성 Nephrotic Syndrome의 Genotype–Phenotype 상관관계
📍핵심 정리
1. CNS·영아성 NS의 50% 이상은 단일유전자 원인을 가지며, NPHS1·NPHS2·WT1·LAMB2 4개 유전자가 전체의 2/3를 설명합니다.
2. 같은 유전자 변이라도 발현 시점이 이를수록(CNS) 더 심한 유전형, 더 빠른 신부전 경과와 연관됩니다.
3. Compound heterozygous NPHS1 변이, NPHS1/WT1 또는 NPHS1/NPHS2 digenic 변이는 이식 필요성과 강하게 연관됩니다.
4. 유전자 검사 결과 없이는 스테로이드 반응성 예측, 이식 전략, 가족상담을 체계적으로 수행하기 어렵습니다.
5. 단일 유전자 검사 음성’은 유전성 배제의 근거가 되지 않으므로, 포괄적 패널 또는 WES를 고려해야 합니다.
같은 진단명, 다른 예후
선천성 nephrotic syndrome(CNS, 생후 0~3개월 발현)과 영아성 nephrotic syndrome(INS, 생후 3~12개월 발현)은 임상 표현이 유사해 보입니다. 그러나 원인 유전자의 종류와 변이 형태에 따라 신부전 도달 시점, 이식 필요 여부, 이식 전 신절제술 고려 여부가 근본적으로 달라집니다.
이 글은 최신 연구들을 바탕으로, 주요 원인 유전자별 표현형 특성을 정리하고 유전자형 정보가 왜 임상 의사결정의 출발점이 되어야 하는지를 논합니다.
1. CNS·영아성 NS의 유전적 구조
CNS와 영아성 NS를 가진 환자의 상당수는 단일유전자 원인을 가지며, 고전적 유럽 코호트에서는 생후 1년 이내 발현 환자의 66.3%가 NPHS1, NPHS2, WT1, LAMB2 네 유전자로 설명되었습니다.
특히 CNS에서는 84.8%, 영아성 NS에서는 44.1%에서 원인 변이가 확인되었습니다.
다만 이 코호트에서는 NPHS2가 양 군 모두에서 가장 흔한 원인 유전자였고, NPHS1 변이는 congenital onset에서만 확인되었습니다.
표 1. 발현 시점에 따른 주요 원인 유전자 분포¹
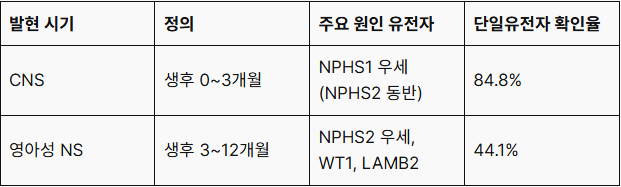
※ NPHS1 변이는 CNS에서만 확인되고 영아성 NS에서는 거의 관찰되지 않습니다.¹
2. 유전자별 표현형 특성
2-1. NPHS1 (Nephrin): 유전자 변이는 예후의 큰 방향을 결정하는 핵심 인자입니다.
NPHS1은 slit diaphragm의 핵심 구조 단백질인 nephrin을 암호화합니다. 일본 다기관 연구(n=74)에서 NPHS1 변이 환자는 다른 유전자 변이 환자에 비해 신부전 도달 시점이 유의미하게 늦었습니다(CNS군 기준 중앙값 31.0개월 vs. 1.0개월, p<0.001).² 그러나 동일 NPHS1 변이 내에서도 CNS 발현 환자가 영아성 NS 발현 환자보다 신부전에 현저히 빠르게 도달했습니다(중앙값 0.5개월 vs. 9.1개월, p<0.001).²
North American PNRC 11개 기관 코호트(n=36) 연구에서는 c.2335-1 G>A와 같은 splice site 변이를 포함한 NPHS1 compound heterozygous 변이가 단백뇨 수치와 관련이 있었으며(112.4±135.6 vs. 53.9±57.3 g/day), 단독 변이 환자보다 더 심한 단백뇨와 관련된 것으로 보고되었습니다.¹ (단, 이 수치는 소규모 코호트 기반으로 해석에 주의가 필요합니다.)
2-2. WT1: 영아성 NS에서 비율이 높고, 변이 위치가 예후를 좌우합니다
WT1 변이는 영아성 NS 그룹에서 상대적으로 더 빈번하게 발견됩니다.¹ 일본 코호트 연구에서 WT1 변이 보유 CNS 환자는 모두 신부전 도달 연령 중앙값이 1.5개월인 반면, 영아성 NS 환자의 경우 15.0개월으로 유의미한 차이가 확인되었습니다(p=0.006).²
변이 위치도 중요합니다. Exon 8 또는 9의 DNA-binding site에 위치한 변이를 보유한 환자는 다른 위치 변이 환자보다 더 심한 신장 예후를 보였으며, Cys2-His2 Zinc finger structure site 변이 역시 severe phenotype과 연관되는 것으로 보고되었습니다.²
또한 ERKNet-ESPN 컨센서스에 따르면, WT1 dominant pathogenic variant를 가진 환자는 이식 전 신절제술 고려가 권고됩니다.³ 이는 유전자 검사 결과가 외과적 의사결정에도 직접 영향을 미치는 사례입니다.
2-3. 발현 시점 자체가 예후 인자입니다
동일 유전자 내에서도 CNS(0~3개월 발현)와 영아성 NS(3~12개월 발현) 간 예후 차이가 일관되게 관찰됩니다. 일본 다기관 연구에서 NPHS1 이외 유전자 변이를 가진 경우, CNS 환자의 신부전 도달 중앙 연령은 1.0개월, 영아성 NS 환자는 15.0개월이었습니다(p<0.001).² 이는 더 이른 발현이 더 심한 유전형(truncating variant, severe missense 등)과 연관될 가능성이 높음을 시사합니다.

3. Digenic·Triallelic 유전: 단일 유전자 검사의 한계
주목해야 할 유형이 있습니다. NPHS1/WT1 또는 NPHS1/NPHS2 두 유전자에 동시에 병원성 변이가 존재하는 digenic 유전의 경우, 단일 유전자 변이 단독 보유 환자에 비해 발현 시점에 관계없이 이식 필요성과 강하게 연관되는 것으로 North American PNRC 코호트에서 보고되었습니다.¹
이는 임상적으로 중요한 함의를 가집니다. 예를 들어 NPHS2 단독 검사에서 음성 결과가 나왔더라도, 동시에 NPHS1 변이가 존재하는 경우 심각한 표현형이 나타날 수 있습니다. ‘단일 유전자 음성’이 ‘유전성 아님’을 의미하지 않으므로, 포괄적 패널 또는 Whole Exome Sequencing(WES)의 필요성이 이러한 데이터로 뒷받침됩니다.
4. 유전자 검사 결과가 바꾸는 임상 의사결정
4-1. 불필요한 면역억제 노출을 막습니다
생후 1년 이내 NS에서 4개 핵심 유전자 변이(NPHS1, NPHS2, WT1, LAMB2)가 확인된 45명의 환자 중 스테로이드에 지속적으로 반응한 사례는 1명에 불과했습니다. 이 데이터는 유전성 NS로 확인된 경우 면역억제제에 대한 반응을 기대하기 어렵다는 점을 보여주며, 장기 스테로이드 노출에 따른 부작용을 예방하기 위해서도 조기 유전자 진단이 필요함을 시사합니다.
4-2. 신장이식 전략 수립에 직접 관여합니다
ERKNet-ESPN 컨센서스 권고안에 따르면, WT1 dominant pathogenic variant를 가진 환자는 신장이식 이전에 신절제술을 고려해야 합니다. 이는 WT1 변이 관련 Wilms 종양 위험성 때문입니다. 반대로 NPHS1 biallelic truncating 변이 환자는 이식 후 항nephrin 항체가 형성될 수 있어, 이식 후 면역 모니터링 전략이 달라집니다. 유전자형을 모른 채로 이식을 결정하는 것은 이러한 위험을 놓칠 수 있습니다.
4-3. 가족 유전상담의 근거가 됩니다
NPHS1과 NPHS2는 모두 상염색체 열성(autosomal recessive) 유전 양식을 따릅니다. 따라서 확진 환자가 발생한 가족에서는 형제자매의 발병 위험이 25%에 달하며, 보인자 부모에 대한 유전상담과 산전 진단의 가능성도 열립니다. 유전자 진단 없이는 이러한 가족 수준의 대응이 불가능합니다.
5. 현재의 한계
이 분야에는 아직 중요한 지식 공백이 존재합니다. 첫째, 단일유전자 원인이 확인되지 않는 CNS·영아성 NS 사례가 여전히 상당 비율을 차지하며, 미발견 원인 유전자가 존재할 가능성이 있습니다. 둘째, Variants of Uncertain Significance(VUS)에 대한 해석은 여전히 도전적인 문제입니다. NPHS1과 CRB2 등의 유전자에서 VUS가 보고되고 있으나, 이러한 변이의 병원성을 확인하기 어려운 경우가 있습니다. 셋째, 아시아·아프리카 등 비유럽 코호트의 변이 데이터베이스 구축이 부족하여, 인종별 특이적 변이 해석에 한계가 있습니다.
선천성·영아성 Nephrotic Syndrome이 의심되는 환자를 진료 중이시라면, 원인 유전자 확인이 첫 번째 임상 결정이 됩니다. 3billion은 Whole Exome Sequencing(WES), Whole Genome Sequencing(WGS)를 자동 재분석 기술과 함께 제공합니다. 아래 버튼을 통해 자세한 정보를 받아보세요.
참고문헌
- Islam MS et al. “Congenital and infantile nephrotic syndrome: genotype-phenotype associations.” Pediatric Research. 2025 – 사용 근거: 발현 시기별 유전자 분포, compound heterozygous NPHS1 변이와 단백뇨 수치, digenic 유전과 이식 연관성
- Inoki Y et al. “Differences in kidney prognosis between congenital and infantile nephrotic syndrome.” Pediatric Nephrology. 2025 — 사용 근거: CNS vs 영아성 NS 간 신부전 도달 중앙값(NPHS1: 31.0 vs. −개월 / 비NPHS1: 1.0 vs. 15.0개월), WT1 변이 위치별 신장 예후, NPHS1 이외 유전자 변이와 발현 시점 상호작용
- Boyer O et al. “Management of congenital nephrotic syndrome: consensus recommendations of the ERKNet-ESPN Working Group.” Nature Reviews Nephrology. 2021;17(4):277-289. — 사용 근거: WT1 dominant pathogenic variant 환자에서 이식 전 신절제술 고려 권고
- Lee JX et al. “NPHS Mutations in Pediatric Patients with Congenital and Steroid-Resistant Nephrotic Syndrome.” International Journal of Molecular Sciences. 2024 Nov 15;25(22). — 사용 근거: NPHS1·NPHS2 변이 유병률 메타분석, 유럽 NPHS2 변이 환자의 ESRF 위험(OR=7.97), 4개 유전자가 생후 1년 이내 NS의 2/3를 설명한다는 근거, 확인된 유전자 변이 보유 환자 45명 중 1명만 스테로이드 반응
- Zafar F et al. “Heterozygous variants of uncertain significance in NPHS1 and CRB2 in a newborn with congenital nephrotic syndrome of the Finnish type and multiple fetal anomalies: a case report.” AME Case Reports. 2025 — 사용 근거: VUS(Variants of Uncertain Significance) 해석의 한계에 관한 임상 사례
- Rong L et al. “Genetic Variations and Clinical Features of NPHS1-Related Nephrotic Syndrome in Chinese Children: A Multicenter, Retrospective Study.” Frontiers in Medicine. 2021;8:771227. — 사용 근거: NPHS1 compound heterozygous 변이가 중국 인구에서 주요 변이 유형임을 보여주는 근거, 인종별 변이 분포 차이 맥락
3billion 뉴스레터 구독자만을 위한
희귀질환 진단 최신 정보를 받아보세요.

Soo-jung Baek
희귀질환 진단이라는 막막한 길 위에서, 정확한 정보와 따뜻한 공감으로 여러분의 여정에 끝까지 함께하고 싶은 마케터 백수정입니다.