Beyond the Variant: Interpreting Genetic Diseases in the AI Era – Episode 3 Ehlers-Danlos Syndrome (EDS)
📌 Series Introduction
이 시리즈는 AI 기반 유전변이 판독 도구가 보편화된 시대에, 자동화된 우선순위화 이후 판독자가 실제로 무엇을 이해하고 어떻게 판단해야 하는지에 초점을 맞춥니다.
각 편에서는 하나의 질환군을 중심으로, 유전적 기전과 임상 스펙트럼을 함께 살펴보며 변이를 “찾는 것”을 넘어 “설명하고 해석하는” 데 필요한 관점을 공유하고자 합니다.
Ehlers-Danlos syndrome(EDS)은 콜라겐과 세포외기질(ECM)의 이상으로 발생하는 유전성 결합조직 질환군입니다.
피부, 관절, 혈관, 근골격계 등 다양한 조직에서 구조적 취약성이 나타나며, 질환의 표현형도 매우 다양하게 나타나는 것이 특징입니다.
이번 Episode 3에서는 EDS의 정의, 분류, 원인 유전자, 분자적 병태생리, 그리고 임상 진단 기준까지 체계적으로 정리합니다.
Episode 3 — Ehlers-Danlos Syndrome (EDS) 관련 질환
🔍 Ehlers-Danlos Syndrome이란?
Ehlers-Danlos syndrome은 결합조직(connective tissue)의 구조적 결함으로 발생하는 희귀 유전 질환군입니다.
질환명은 두 명의 피부과 의사에서 유래했습니다.
- Edvard Ehlers
- Henri-Alexandre Danlos
이 질환의 핵심 특징은 다음과 같습니다.
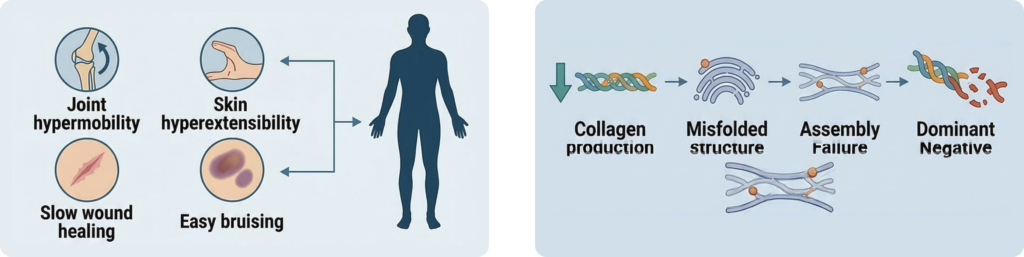
주요 임상 특징
- 관절 과운동성 (Joint hypermobility)
- 피부 과신전 (Skin hyperextensibility)
- 비정상적인 상처 치유
- 쉽게 생기는 멍 (Easy bruising)
결합조직은 인체 대부분의 장기에서 구조적 지지 역할을 하기 때문에, EDS는 단순 피부 질환이 아니라 전신적인(multisystem) 결합조직 질환입니다.
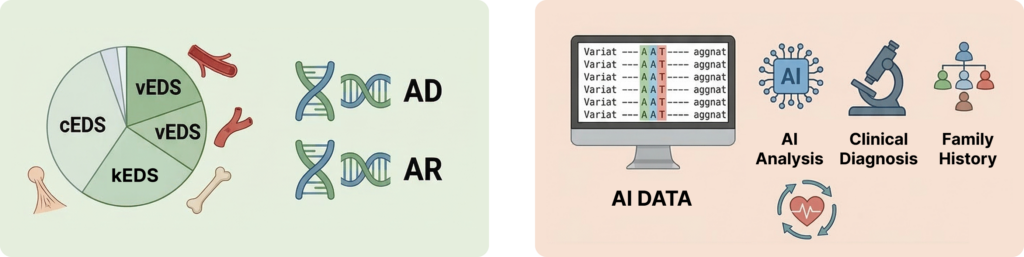
🧬 Ehlers-Danlos Syndrome 분류
현재 국제적으로 14개의 EDS subtype이 정의되어 있습니다.
대표적인 유형은 다음과 같습니다.
- Classical EDS (cEDS)
- Vascular EDS (vEDS)
- Kyphoscoliotic EDS (kEDS)
- Myopathic EDS (mEDS)
- Periodontal EDS (pEDS)
이 중 13개 subtype은 유전자 원인이 밝혀져 있으며,
Hypermobile EDS (hEDS)만이 아직 분자적 원인이 명확히 밝혀지지 않았습니다.
EDS 발생률
EDS subtype별 발생률의 예시는 다음과 같습니다
- Classical EDS: 약 1 / 20,000
- Vascular EDS: 약 1 / 50,000 – 1 / 200,000
일부 subtype은 매우 드문 희귀질환에 해당합니다.
🧐 EDS 원인: 어떤 유전자 변이가 발생할까?
현재까지 20개의 유전자가 EDS와 관련되어 있습니다.
대표적인 유전자는 다음과 같습니다.
| COL5A1 | COL5A2 | COL1A1 | COL3A1 | |||
| COL1A2 | ADAMTS2 | PLOD1 | FKBP14 | |||
| TNXB | COL12A1 | CHST14 | DSE | |||
| B4GALT7 | B3GALT6 | SLC39A13 | ZNF469 | |||
| PRDM5 | C1R | C1S | AEBP1 |
EDS의 유전 방식은 다음과 같습니다.
- 상염색체 우성 (Autosomal dominant)
- 상염색체 열성 (Autosomal recessive)
이 유전자들은 기능적으로 크게 세 가지 범주로 나뉩니다.
1. Fibrillar collagen 단백질
- COL1A1
- COL3A1
- COL5A1
- COL5A2
2. Collagen processing 효소
- ADAMTS2
- PLOD1
- FKBP14
3. ECM 및 proteoglycan 관련 단백질
- TNXB
- B4GALT7
- CHST14
- DSE
이러한 유전자 변이는 모두 콜라겐 구조 또는 세포외기질(ECM)의 안정성에 영향을 미칩니다.
📌 콜라겐 구조와 EDS의 분자적 기전
EDS를 이해하려면 먼저 콜라겐의 기본 구조를 이해해야 합니다.
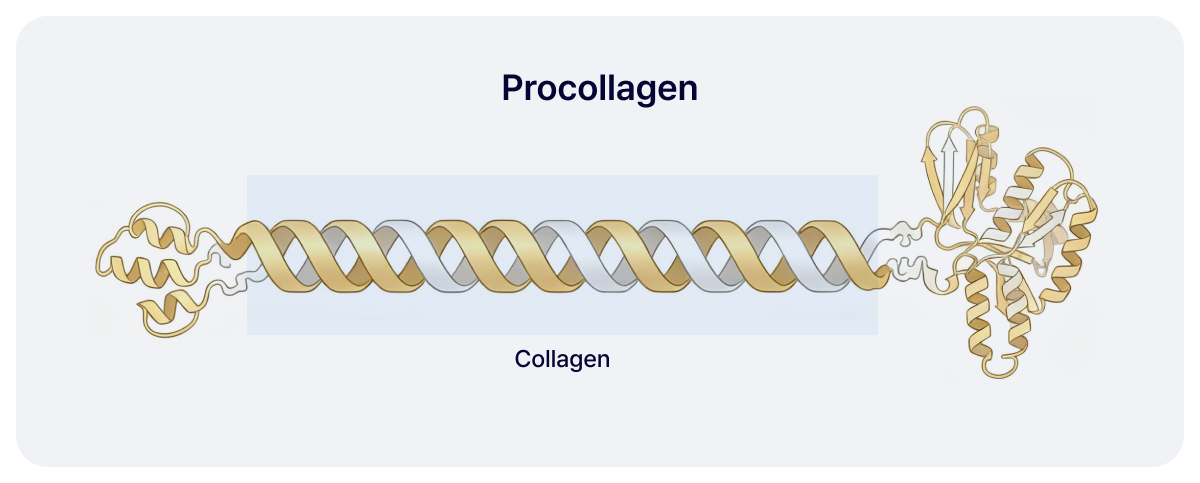
콜라겐 triple helix 구조
콜라겐은 세포 내에서 프로콜라겐(procollagen) 형태로 합성된 후, proteolytic cleavage를 거쳐 성숙한 콜라겐(mature collagen)으로 전환됩니다.
프로콜라겐은 세 개의 폴리펩타이드 α-chain으로 구성되며, 이들이 결합하여 삼중 나선(triple helix) 구조를 형성합니다.
이 구조는 동일한 사슬로 이루어진 homotrimer 또는 서로 다른 사슬로 이루어진 heterotrimer 형태로 존재할 수 있습니다.
Triple helix domain의 중심부에는 다음과 같은 특징적인 반복 서열이 존재합니다.
Gly–X–Y motif
- Gly: glycine
- X / Y: 주로 proline 또는 hydroxyproline
이러한 반복 구조는 콜라겐의 안정적인 triple helix 구조 형성에 필수적입니다.
프로콜라겐은 이후 proteolytic cleavage를 통해 N- 및 C-말단 propeptide가 제거되며, 그 결과 성숙한 콜라겐 분자(mature collagen molecules)가 형성됩니다.
Classical EDS 원인
Classical EDS는 Type V collagen 결함으로 발생합니다.
Type V collagen은 heterotrimer 구조로 이루어져 있으며, 하나의 heterotrimer는 두 개의 α1(V) chain과 한 개의 α2(V) chain으로 구성됩니다.
이러한 α-chain을 암호화하는 유전자는 다음과 같습니다.
- α1(V): COL5A1
- α2(V): COL5A2
→ 콜라겐 섬유 형성(collagen fibrillogenesis)에 필수적인 역할을 합니다.
1. COL5A1 변이 특징
대부분 haploinsufficiency
주요 변이
- nonsense
- frameshift
이 변이는 NMD (nonsense mediated decay)를 유발합니다.
결과적으로 정상 collagen V 생산이 약 50% 감소합니다.
2. COL5A2 변이 특징
COL5A2에서는
- missense
- in-frame indel
같은 구조적 변이가 주로 발견됩니다.
이러한 변이는 collagen 구조 자체를 직접 손상시키기 때문에 종종 더 심한 임상 표현형을 유발합니다.
Vascular EDS 원인
Vascular EDS는 COL3A1 유전자 변이로 발생합니다.
Type III collagen은 homotrimer 구조를 가지며, 세 개의 동일한 α1(III) chain으로 구성됩니다
- collagen fibril assembly
- fibril diameter 조절
에 중요한 역할을 합니다.
대표적인 병리 기전은 다음과 같습니다.
- glycine substitution
- in-frame indel
in the triple helical domain
이 변이는
- dominant negative collagen misfolding
- ER retention
- secretion failure
을 유발합니다.
그 결과 ECM 구조가 약화되어
- 혈관 파열
- 장기 파열
같은 심각한 합병증이 발생할 수 있습니다.
Type I collagen 관련 EDS
Type I collagen은 ECM에서 가장 풍부한 단백질입니다.
Type I collagen은 heterotrimer 구조를 가지며, 두 개의 α1(I) chain과 하나의 α2(I) chain으로 구성됩니다.
관련 유전자
- COL1A1
- COL1A2
대부분의 변이는 osteogenesis imperfecta를 유발하지만 일부는 EDS subtype을 유발합니다. 주요 병리 기전은 N-propeptide cleavage 및 procollagen processing 과정의 이상으로 인해 정상적인 collagen fibrillogenesis가 이루어지지 않는 것입니다.
대표적인 예:
Arthrochalasia EDS (aEDS)
- 이형접합 COL1A1 / COL1A2 변이
(exon 6 부분 또는 전체 결실) - N-propeptide cleavage site 소실
- Cross-linking lysine / protease cleavage site / 초기 triple-helix triplet 소실
- Type I procollagen의 N-terminal이 제거되지 않고 일부 남음
- Procollagen processing 이상 발생
→ Collagen fibrillogenesis 장애
특징
- 심한 관절 과운동성
- 선천성 고관절 탈구
Dermatosparaxis EDS (dEDS)
원인
ADAMTS2 변이/양쪽 대립유전자 ADAMTS2 기능 소실 (biallelic loss)
Procollagen N-cleavage 실패
비정상적인 콜라겐 섬유 형성
특징
- extreme skin fragility
- severe bruising
전자현미경에서 hieroglyphic collagen fibril 형태가 관찰됩니다.
aEDS와 dEDS의 표현형 차이는 protease redundancy에 의해 설명됩니다.
(ADAMTS3,ADAMTS14 등 다른 효소가 일부 기능을 보완)
또한 ADAMTS2는 다양한 기질(substrate)을 처리하는 효소입니다.
→ 이러한 차이가 질환의 표현형 차이에 영향을 미칩니다.
Type I collagen 관련 다른 EDS 기전도 있습니다.
Cardiac valvular EDS (cvEDS)
- biallelic COL1A2 loss-of-function 변이
- NMD에 의해 mRNA 불안정 → proα2(I) chain 결핍
- α1(I) homotrimer collagen 형성
- 심한 다판막 심장질환 발생
대조되는 기전
- biallelic COL1A2 LoF이지만 mRNA가 안정적인 경우
- 불안정한 단백질 → UPR (ER stress) 활성화
- 경도–중등도 Osteogenesis imperfecta 발생
→ ECM 이상 vs ER stress 기반 병리 기전 차이
COL1A1 Arg → Cys 변이
- 이형접합 COL1A1 Arg→Cys 치환 변이
- Triple helix에 cysteine 도입 → 비정상적인 disulfide-bond dimer 형성
- 국소적인 collagen 구조 불안정 및 ECM 상호작용 변화
- vEDS와 유사한 동맥 파열 위험 ± cEDS 유사 피부/관절 증상
표현형 스펙트럼
- 일부 변이 → COL5 변이 없이 cEDS 유사 표현형
- 다른 변이 → EDS / OI overlap (관절 과이완 + 경한 골 취약성)
Collagen crosslinking 이상: kEDS
Collagen fibrillogenesis 단계뿐 아니라, collagen의 folding 및 cross-linking 과정에 이상이 발생해도 EDS가 나타날 수 있습니다. 이러한 경우 주로 kyphoscoliotic EDS 형태로 발현됩니다.
Kyphoscoliotic EDS (kEDS)
Kyphoscoliotic EDS는 두 가지 유전자에서 발생합니다.
PLOD1
lysyl hydroxylase 결핍 → collagen crosslinking 장애
약 30%의 변이는 exon 10–16 중복으로 발생하며, 이는 Alu-mediated recombination에 의해 발생합니다.
임상 특징
- progressive scoliosis
- vascular fragility
FKBP14
ER chaperone 단백질 → collagen folding 장애
결과
- ER collagen accumulation
- abnormal fibril formation
Founder frameshift variant가 대부분의 alleles를 차지합니다.
ECM 구조 단백질 결함
일부 EDS subtype은 collagen 자체의 이상이 아니라, collagen 주변의 다른 ECM organizing protein의 이상으로 발생합니다
Classical-like EDS
원인
- TNXB
양쪽 대립유전자 TNXB 기능소실 변이 (biallelic LoF)
→ Tenascin-X 결핍 발생
결과
- collagen fibril organization 장애
증상
피부 과신전성 (위축성 흉터 없음)
- 멍이 잘 듦, 관절 과운동성 ± 근력 약화
이형접합 보인자 (heterozygotes)
- TNX 감소
- 일부에서 관절 과운동성 (드물게 hEDS와 연관 보고)
Myopathic EDS
원인
- COL12A1
이형접합 또는 양쪽 대립유전자 변이 (COL12A1, type XII collagen)
특징
- EDS + 근육병증
양쪽 대립유전자 변이(biallelic)에서는 심한 선천성 형태로 나타나며, 이형접합 변이(heterozygous)에서는 보다 경한 표현형으로 나타납니다.
Glycosaminoglycan 합성 이상
Proteoglycan은
- ECM 구조 유지
- Collagen 간격 조절 (collagen spacing)
- Cell signaling 조절
등 여러 과정에서 중요한 역할을 합니다.
Proteoglycan은 core protein과 GAG chains (HS, CS, DS)로 구성되어 있으며, GAG chain 합성 과정에 이상이 발생하면 EDS가 발생할 수 있습니다.
Spondylodysplastic EDS
원인
B4GALT7
B3GALT6
GAG chain 합성은 core protein에 tetrasaccharide linker가 부착되는 과정에서 시작됩니다. 이 과정에서 B4GALT7 또는 B3GALT6 변이가 발생하면 linker의 galactosylation에 문제가 생깁니다.
그 결과
- core protein에 당(sugar)을 정상적으로 추가할 수 없게 되고
- HS (heparan sulfate) 및 CS (chondroitin sulfate)가 감소하거나 짧아지며
- decorin에서 DS (dermatan sulfate)가 소실됩니다.
특징
- skeletal dysplasia
- hypotonia
Musculocontractural EDS
원인
- CHST14
- DSE
CHST14 또는 DSE 유전자에 양쪽 대립유전자 변이(biallelic variants)가 발생하면 DS(dermatan sulfate) 합성에 장애가 생깁니다. 이로 인해 DS가 감소하거나 소실되며, 그 자리를 CS(chondroitin sulfate)가 대신하게 됩니다.
그 결과 decorin의 정상적인 기능이 손상(dysfunction)되어 ECM 구조와 collagen 조직화에 문제가 발생합니다.
특징
- congenital contracture
- craniofacial anomalies
Other Intracellular Molecules 결함
spEDS (SLC39A13-related)
- 양쪽 대립유전자 SLC39A13 변이
- ZIP13 zinc transporter 기능 이상 → 세포질로의 zinc 유입 감소
그 결과
- Collagen lysyl / prolyl hydroxylation 감소
→ ECM crosslinking 이상
추정 기전
- Zn / Fe 불균형
- lysyl hydroxylase, prolyl hydroxylase와 경쟁적 결합
- ER stress
- BMP / TGFβ signaling 변화
→ 최종적으로 collagen modification 이상과 결합조직 안정성 저하 발생
Brittle Cornea Syndrome (BCS)
- 양쪽 대립유전자 ZNF469 또는 PRDM5 변이
주요 특징
- 매우 얇고 취약한 각막
→ 각막 파열 위험 증가
PRDM5 기능
- ECM 유전자 발현을 조절하는 전사 조절 인자
그 결과
- ECM 유전자 발현 이상
→ collagen, fibronectin, integrin 침착(deposition) 변화
Complement pathway 관련 EDS
Periodontal EDS
- 이형접합 C1R 또는 C1S 변이
(classical complement pathway 관련 유전자)
주요 특징
- 심한 치주염 (aggressive periodontitis)
- 조기 치아 상실
- 경한 관절 과운동성
병리 기전
- C1 protease의 GoF 활성화
→ 국소적인 complement 활성 증가
추정 기전
- CUB domain을 통한 ECM / collagen과의 비정상적 상호작용
→ 면역계와 결합조직 간 상호작용의 중요성 시사
Periodontal EDS
- 양쪽 대립유전자 AEBP1 변이
→ ACLP (collagen-binding ECM protein) 소실
주요 특징
- 피부 과신전성 및 위축성 흉터
- 관절 과운동성
- 골감소증(osteopenia)
병리 기전
- Collagen I polymerization 이상
추정 기전
- TGFβ signaling 변화 (fibroblast 전환 영향)
- Wnt signaling 변화 (골 항상성 영향)
→ 정확한 병리 기전은 아직 완전히 규명되지 않습니다.
EDS 진단 방법
EDS 진단 시 다음 특징들을 평가합니다.
공통 특징
- generalized joint hypermobility
- skin hyperextensibility
- easy bruising
- abnormal wound healing
- tissue fragility
또한 가족력 평가와 전신적 임상 평가가 중요합니다.
EDS 진단이 어려운 이유
EDS는 특히 소아에서 진단이 늦어지는 경우가 많습니다.
그 이유는 다음과 같습니다.
- 조직 취약성이 정상 범위로 오해될 수 있음
- 피부 과신전이 피하지방에 의해 가려질 수 있음
- 멍이나 피부 손상은 보행 이후 나타나는 경우가 많음
또한 vEDS의 혈관 파열 같은 심각한 합병증은 대개 청소년기 이후 나타나는 경우가 많습니다.
References
Malfait, F. et al. The Ehlers–Danlos syndromes. Nat. Rev. Dis. Primers 6, 64 (2020).
Malfait, F. et al. The 2017 international classification of the Ehlers–Danlos syndromes. Am. J. Med. Genet. C Semin. Med. Genet. 175, 8–26 (2017).
Blackburn, P. R. et al. Bi-allelic alterations in AEBP1 lead to defective collagen assembly and connective tissue structure resulting in a variant of Ehlers–Danlos syndrome. Am. J. Hum. Genet. 102, 696–705 (2018).
Wenstrup, R. J. et al. What mouse mutants teach us about extracellular matrix function. Annu. Rev. Cell Dev. Biol. 22, 591–621 (2006).
Gao, L., Orth, P., Cucchiarini, M. & Madry, H. Effects of solid acellular type-I/III collagen biomaterials on chondrogenesis of mesenchymal stem cells. Expert Rev. Med. Devices (2017).
Zhang, X. et al. Procollagen-lysine 2-oxoglutarate 5-dioxygenase 2 promotes collagen cross-linking and ECM stiffening to induce liver fibrosis. Biochim. Biophys. Acta Mol. Basis Dis. 1870, 167205 (2024).
Lloyd, S. M. & He, Y. Exploring extracellular matrix crosslinking as a therapeutic approach to fibrosis. Cells 13, 438 (2024).
doi:10.3390/cells13050438
Ishikawa, Y. & Bächinger, H. P. A substrate preference for the rough endoplasmic reticulum resident protein FKBP22 during collagen biosynthesis. J. Biol. Chem. 289, 18189–18201 (2014).
Lethias, C. et al.
A model of tenascin-X integration within the collagenous network.
FEBS Lett. 580, 6281–6285 (2006)
Nguyen, M. & Panitch, A. Proteoglycans and proteoglycan mimetics for tissue engineering. Am. J. Physiol. Cell Physiol. 322, C754–C761 (2022).
Ruiz Martínez, M. A., Peralta Galisteo, S., Castán, H. & Morales Hernández, M. E. Role of proteoglycans on skin ageing: a review. Int. J. Cosmet. Sci. 42, 529–535 (2020).
Green, C. et al. Classical-like Ehlers–Danlos syndrome: a clinical description of 20 newly identified individuals with evidence of tissue fragility. Genet. Med. 22, 1576–1582 (2020).
Abdalla, E. M. et al. Kyphoscoliotic type of Ehlers–Danlos syndrome (EDS VIA) in six Egyptian patients presenting with a homogeneous clinical phenotype. Eur. J. Pediatr. 174, 105–112 (2015).
Chen, Y. et al. Role of genetics in amyotrophic lateral sclerosis: a large cohort study in Chinese mainland population. J. Med. Genet. 59, 840–849 (2022).
3billion 뉴스레터 구독자만을 위한
희귀질환 진단 최신 정보를 받아보세요.

3billion Inc.
희귀질환 환자들이 진단과 치료에서 외면받지 않는 세상을 만들기 위해 쓰리빌리언은 하나의 미션을 바라봅니다.