Episode 7: Prader-Willi and Angelman Syndromes — Beyond the Variant
📌 Series Introduction
이 시리즈는 3billion의 임상 유전학 전문가가 직접 작성한 글입니다.
AI 기반 유전변이 판독 도구가 보편화된 시대에, 자동화된 우선순위화 이후 판독자가 실제로 무엇을 이해하고 어떻게 판단해야 하는지에 초점을 맞춥니다.
각 편에서는 하나의 질환군을 중심으로, 유전적 기전과 임상 스펙트럼을 함께 살펴보며 변이를 “찾는 것”을 넘어 “설명하고 해석하는” 데 필요한 관점을 공유하고자 합니다.
Key Takeaway
- Prader-Willi syndrome(PWS)과 Angelman syndrome(AS)은 모두 15q11-q13 imprinting region과 관련된 질환이다.
- 두 질환의 핵심 차이는 genomic location 자체보다 parent-of-origin effect에 있다.
- PWS는 주로 paternal gene expression loss와 관련되며, SNORD116이 중요한 역할을 한다.
- AS는 neuron에서의 maternal UBE3A 기능 소실이 핵심이다.
- Imprinting disorder의 variant interpretation에서는 phenotype, methylation, inheritance 정보를 함께 고려해야 한다.
같은 15q11-q13, 다른 결론: PWS와 Angelman Syndrome이 판독자에게 주는 메시지
Prader-Willi syndrome(PWS)과 Angelman syndrome(AS)은 모두 15q11-q13 영역과 관련된 대표적인 imprinting disorder입니다.
흥미로운 점은 두 질환이 같은 염색체 영역에서 시작되지만, 임상 양상은 완전히 다르다는 것입니다.
차이를 만드는 핵심은 단순히 “어떤 영역이 없어졌는가”가 아니라, 어느 부모로부터 유래한 allele이 영향을 받았는가입니다.
부계 유래 15q11-q13 영역의 기능이 소실되면 Prader-Willi syndrome(PWS)가 발생하고, 모계 유래 UBE3A 기능이 소실되면 Angelman syndrome(AS)가 발생합니다.
즉, 이 두 질환은 판독자에게 중요한 질문을 던집니다.
“이 variant 또는 CNV가 어디에 있는가?”만으로 충분한가? 아니면 “이 변화가 어떤 유전적·후성유전학적 맥락에서 질환으로 이어지는가?” 까지 봐야 하는가?
PWS와 AS는 왜 다르게 나타날까요?
임프린팅 조절과 전사 시작의 차이
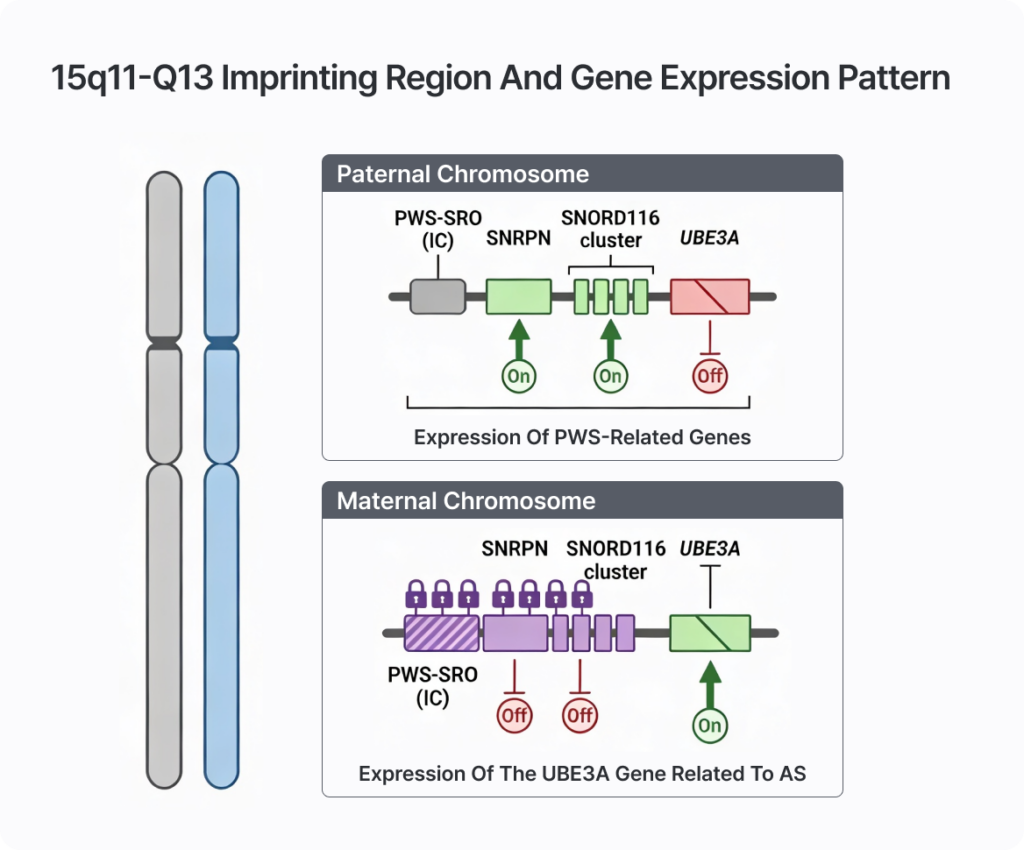
15q11-q13 영역은 부모 유래에 따라 서로 다른 유전자가 발현되는 대표적인 imprinting region입니다.
즉, 동일한 DNA 서열을 가지고 있더라도, 해당 염색체가 부계에서 유래했는지 모계에서 유래했는지에 따라 특정 유전자의 발현 여부가 달라집니다. 이러한 parent-of-origin specific expression은 DNA methylation을 중심으로 한 epigenetic regulation에 의해 조절됩니다.
이 영역에서 imprinting의 핵심 역할을 하는 부위는 PWS-SRO (Prader-Willi syndrome smallest region of overlap) 로 알려진 imprinting center(IC)입니다. 해당 영역은 PWS 발생에 가장 핵심적인 최소 공통 결실 부위이며, 동시에 SNRPN 유전자 전사가 시작되는 중요한 조절 구간입니다.
현재까지 알려진 모델에 따르면, 부계와 모계에서 imprinting pattern이 달라지는 중요한 이유 중 하나는 전사(transcription)의 시작 위치가 서로 다르기 때문입니다.
부계 염색체에서는 일반적인 exon에서 전사가 시작되지만, 모계 염색체에서는 그보다 upstream에 위치한 alternative exon 1에서 전사가 시작됩니다. 이 과정에서 PWS-SRO 영역에 존재하는 CpG island가 중요한 역할을 하게 됩니다.
특히 모계에서 alternative exon 1으로부터 시작된 전사는 인접한 PWS-SRO 영역에 methylation이 형성되도록 유도하는 신호로 작용하는 것으로 알려져 있습니다. 정확한 기전은 아직 완전히 규명되지는 않았지만, 현재는 transcription process 자체가 chromatin structure를 변화시키면서 methylation이 잘 형성될 수 있는 환경을 만든다는 모델이 널리 받아들여지고 있습니다.
즉, RNA polymerase가 해당 영역을 지나가면서 chromatin accessibility와 nucleosome organization을 변화시키고, 그 결과 DNA methyltransferase가 접근하기 쉬운 상태가 형성되어 CpG island methylation이 유도된다는 것입니다. 실제로 모계에서 alternative exon 1 영역을 제거하면 정상적인 imprint methylation establishment가 이루어지지 않는다는 보고도 존재합니다. 결국 매우 작은 transcription start site의 차이가 이후의 methylation state와 유전자 발현 패턴 전체를 결정하게 되는 것입니다.
이렇게 형성된 서로 다른 methylation pattern은 부계와 모계 염색체에서 전혀 다른 유전자 발현 결과를 만들어냅니다.
부계 발현 소실과 PWS의 병태생리
부계 염색체에서는 PWS region promoter가 unmethylated 상태를 유지하기 때문에 SNRPN, SNORD116 cluster 등을 포함한 여러 paternally expressed gene들이 활발하게 발현됩니다. 반면 모계 염색체에서는 해당 promoter 영역이 methylated state로 유지되어 이들 유전자들의 전사가 억제됩니다.
특히 SNORD116은 PWS의 hyperphagia와 hypothalamic dysfunction에 중요한 역할을 하는 핵심 영역입니다. 실제로 Snord116 결손 마우스 모델에서는 PWS와 유사한 과식 및 대사 이상이 재현되었다는 보고도 있습니다.
UBE3A와 엔젤만 증후군의 ‘충돌 모델’
반면 Angelman syndrome(AS)에서는 UBE3A 유전자가 핵심적인 역할을 합니다.
UBE3A는 대부분 조직에서는 양쪽 allele이 모두 발현되지만, 신경계 특히 neuron에서는 주로 모계 유래 allele만 기능적으로 발현됩니다.
그 이유는 부계 염색체에서 UBE3A-ATS(antisense transcript)가 길게 전사되기 때문입니다. 이 antisense transcript는 UBE3A와 반대 방향으로 전사되며, 결과적으로 부계 UBE3A의 발현을 억제하게 됩니다.
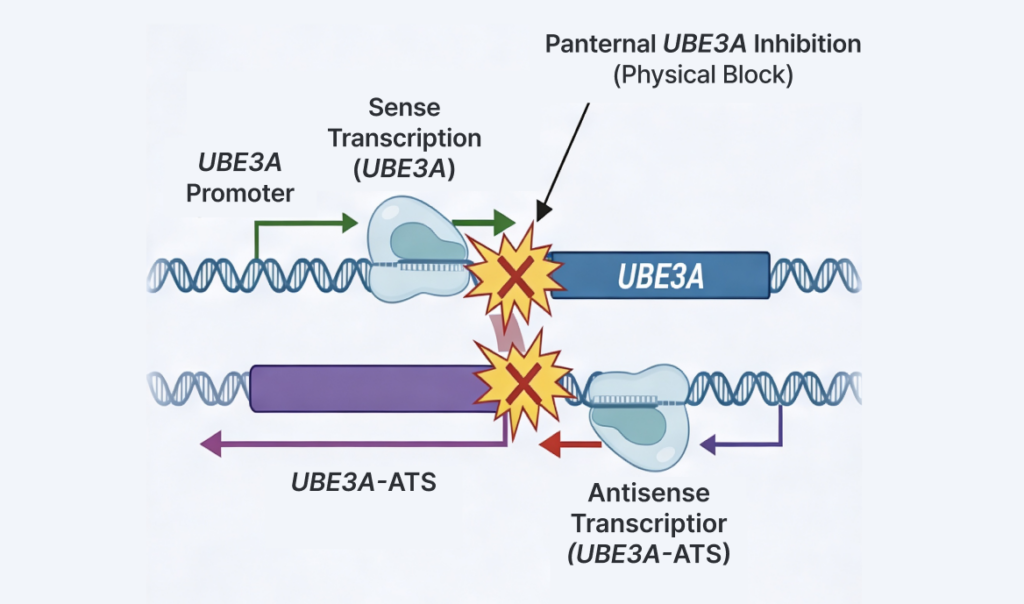
가장 잘 알려진 설명 모델 중 하나는 “collision model”입니다. 이 모델에서는 sense 방향의 UBE3A transcription과 antisense 방향의 UBE3A-ATS transcription이 서로 반대 방향으로 진행되다가 RNA polymerase 간 충돌(transcriptional collision)이 발생한다고 설명합니다. 이 과정에서 UBE3A transcription elongation이 물리적으로 방해받게 되고, 결국 부계 염색체에서는 기능적인 UBE3A 단백질이 거의 생성되지 않게 됩니다.
따라서 정상적인 상황에서는 신경계에서 모계 UBE3A가 사실상 유일한 기능성 UBE3A source 역할을 하게 됩니다. 이 때문에 모계 UBE3A 기능이 소실되면 보상 가능한 UBE3A 발현이 거의 남지 않게 되고, 결과적으로 발달 지연, 중증 언어 장애, 보행 실조, 발작, 특징적인 행동 양상 등 Angelman syndrome의 주요 신경학적 표현형으로 이어질 수 있습니다.
이러한 parent-specific expression pattern이 깨질 경우 Prader-Willi syndrome (PWS) 또는 Angelman syndrome(AS)이 발생하게 됩니다.
대표적인 원인은 다음과 같습니다.
- Deletion: 15q11-q13 영역 자체가 결실되는 경우
- Uniparental disomy (UPD): 동일 부모로부터 두 개의 염색체를 모두 물려받는 경우
- Imprinting defect / imprinting center variant: 정상적인 methylation imprint가 형성되지 못하는 경우
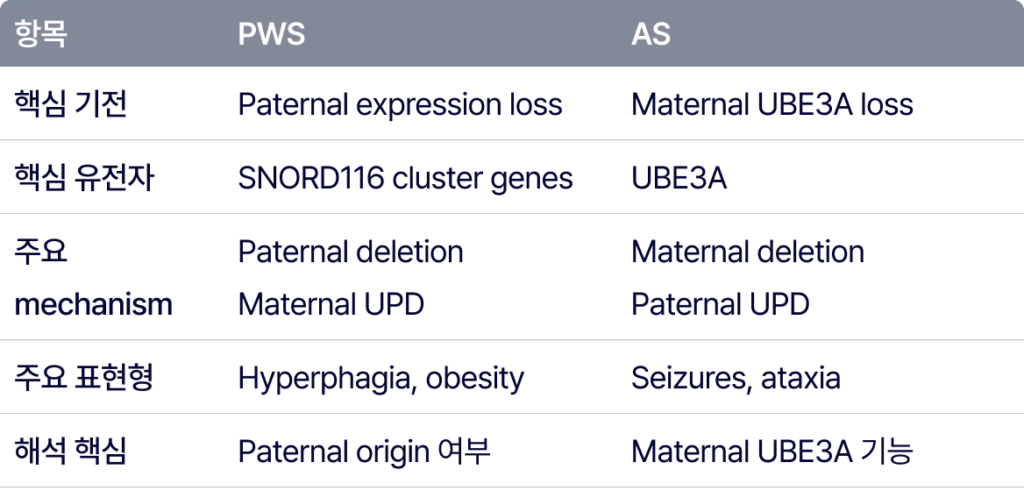
PWS에서는 부계에서 발현되어야 하는 유전자들이 기능을 잃는 것이 핵심입니다. 따라서 부계 15q11-q13 deletion, 모계 UPD(두 개 모두 모계 유래), 혹은 부계 imprint가 정상적으로 형성되지 않는 imprinting defect가 발생하면 PWS가 나타날 수 있습니다.
반대로 AS에서는 neuron에서 기능적으로 발현되는 모계 UBE3A 기능이 소실되는 것이 핵심입니다. 따라서 모계 15q11-q13 deletion, 부계 UPD(두 개 모두 부계 유래), imprinting defect, 혹은 UBE3A 자체의 pathogenic variant 등에 의해 Angelman syndrome이 발생할 수 있습니다.
즉, PWS와 AS는 동일한 염색체 영역의 이상으로 발생하지만, 어떤 parent-specific gene expression이 소실되었는지에 따라 완전히 다른 질환 표현형으로 이어지는 대표적인 genomic imprinting disorder라고 할 수 있습니다.
판독에서 중요한 것은 “variant type”만이 아닙니다.
PWS와 AS는 CNV, UPD, imprinting defect, single-gene variant 등 여러 기전으로 발생할 수 있습니다.
따라서 실제 판독에서는 다음과 같은 질문이 중요합니다.
- 15q11-q13 영역의 deletion인가?
- deletion이 있다면 paternal origin인가, maternal origin인가?
- UPD 가능성은 있는가?
- methylation abnormality가 의심되는가?
- UBE3A single-nucleotide variant 가능성은 있는가?
- 환자의 phenotype이 PWS 쪽에 가까운가, AS 쪽에 가까운가?
같은 region이라도, parent-of-origin effect와 phenotype context에 따라 해석은 완전히 달라집니다.
이 지점에서 PWS와 AS는 단순한 “유전질환 예시”가 아니라, 실제 판독자가 매일 마주하는 문제를 잘 보여줍니다.
즉, variant detection 과 variant interpretation은 서로 다른 문제입니다.
Phenotype context가 해석을 바꿉니다.
PWS는 신생아기 hypotonia, 이후 hyperphagia, 비만, 성장 지연, 근육량 감소 등이 중요한 임상 단서가 됩니다.
AS는 초기에는 비특이적일 수 있지만, 시간이 지나면서 발달 지연, 언어 발달 장애, 보행 실조, 발작, 특징적인 행동 양상이 뚜렷해지는 경우가 많습니다.
따라서 15q11-q13 영역의 CNV가 발견되었다고 해서 바로 PWS 또는 AS로 해석할 수는 없습니다.
실제 interpretation에서는:
- Phenotype
- Onset
- Inheritance
- Methylation pattern
- Parent-of-origin
을 함께 고려해야 합니다.
이 과정은 단순 필터링으로 끝나기 어렵습니다. 판독자는 여러 evidence layer를 연결해야 합니다.
해석은 점점 더 “구조화된 reasoning”이 됩니다.
PWS와 AS는 현대 유전질환 판독이 어디로 가고 있는지를 잘 보여줍니다.
이제 판독은 단순히 pathogenic variant를 찾는 과정이 아닙니다.
- variant type
- genomic region
- parent-of-origin
- methylation/imprinting mechanism
- gene function
- phenotype match
- inheritance pattern
- 기존 보고 사례
- 추가 확인 검사 필요성
이 모든 정보를 종합해 “이 결과가 환자를 설명하는가?”를 판단하는 과정입니다.
특히 imprinting disorder처럼 mechanism이 중요한 질환에서는, 판독자가 evidence를 구조화해서 볼 수 있어야 합니다.
GEBRA는 판독자가 생각할 공간을 더 넓힙니다
GEBRA는 WES/WGS 데이터를 기반으로 variant prioritization, phenotype matching, ACMG evidence, CNV analysis, internal evidence review를 하나의 workflow 안에서 연결합니다.
PWS와 AS처럼 단순 variant detection을 넘어 mechanism과 phenotype context가 중요한 질환에서는, 판독자가 여러 evidence를 흩어진 상태로 확인하는 것보다 구조화된 화면에서 함께 검토하는 것이 중요합니다.
GEBRA가 실제 판독 workflow에서 어떻게 reasoning을 구조화하는지 확인해보세요.
FAQ
Q1. Prader-Willi syndrome(PWS)과 Angelman syndrome(AS)의 가장 큰 차이는 무엇인가요?
A. PWS와 AS는 모두 15q11-q13 imprinting region과 관련된 질환이지만, 어떤 부모 유래 allele이 영향을 받았는지에 따라 완전히 다른 질환으로 이어집니다. PWS는 주로 paternal gene expression loss와 관련되며, AS는 neuron에서의 maternal UBE3A 기능 소실이 핵심입니다.
Q2. 왜 parent-of-origin effect가 variant interpretation에서 중요한가요?
A. 15q11-q13 영역에서는 부모 유래에 따라 발현되는 유전자가 다르기 때문입니다. 같은 deletion이나 CNV라도 paternal origin인지 maternal origin인지에 따라 PWS 또는 AS처럼 서로 다른 표현형으로 이어질 수 있습니다. 따라서 variant interpretation에서는 genomic location뿐 아니라 parent-of-origin, methylation status, phenotype context를 함께 고려해야 합니다.
Q3. Angelman syndrome에서 UBE3A는 왜 중요한가요?
A. UBE3A는 신경계에서 주로 maternal allele만 기능적으로 발현되는 유전자입니다. 반면 paternal UBE3A는 UBE3A-ATS라는 antisense transcript에 의해 억제됩니다. 따라서 maternal UBE3A 기능이 소실되면 neuron에서 보상 가능한 UBE3A 발현이 거의 남지 않게 되고, 발달 지연, 언어 장애, 발작, 보행 실조 등의 Angelman syndrome 표현형이 나타날 수 있습니다.
Q4. GEBRA는 PWS와 AS 같은 imprinting disorder 해석에 어떻게 도움을 줄 수 있을까요?
A. GEBRA는 variant prioritization, phenotype matching, ACMG evidence, CNV analysis를 하나의 workflow 안에서 연결해, 판독자가 복잡한 유전학적 근거를 구조화된 방식으로 검토하고 해석할 수 있도록 돕습니다.
References
- Holm VA, Cassidy SB, Butler MG, Hanchett JM, Greenswag LR, Whitman BY, Greenberg F. Prader-Willi syndrome: consensus diagnostic criteria. Pediatrics. 1993;91(2):398-402. PMID: 8424017; PMCID: PMC6714046.
- Cassidy SB, Schwartz S, Miller JL, Driscoll DJ. Prader-Willi syndrome. Genet Med. 2012;14(1):10-26. doi:10.1038/gim.0b013e31822bead0.
- Driscoll DJ, Miller JL, Schwartz S, Cassidy SB. Prader-Willi Syndrome. In: Adam MP, Feldman J, Mirzaa GM, Pagon RA, Wallace SE, Bean LJH, Gripp KW, Amemiya A, editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle GeneReviews; 1998–2025. Updated 2024 Mar 14. Available from: NCBI Bookshelf NBK1144
- Roberts CT, Arezoumand KS, Kadar Shahib A, Davie JR, Rastegar M. Epigenetics in rare neurological diseases. Front Cell Dev Biol. 2024;12:1413248. doi:10.3389/fcell.2024.1413248. PMID: 39108836; PMCID: PMC11300358
. - Ma VK, Mao R, Toth JN, Fulmer ML, Egense AS, Shankar SP. Prader-Willi and Angelman syndromes: mechanisms and management. Appl Clin Genet. 2023;16:41-52. doi:10.2147/TACG.S372708. PMID: 37051256; PMCID: PMC10084876.
- Mapendano CK, Kishino T, Miyazaki K, Kondo S, Yoshiura KI, Hishikawa Y, Koji T, Niikawa N, Ohta T. Expression of the Snurf-Snrpn IC transcript in the oocyte and its putative role in the imprinting establishment of the mouse 7C imprinting domain. J Hum Genet. 2006;51(3):236-243. doi:10.1007/s10038-005-0351-8. PMID: 16429232.
- Groh M, Gromak N. Out of balance: R-loops in human disease. PLoS Genet. 2014;10(9):e1004630. doi:10.1371/journal.pgen.1004630. PMID: 25233079; PMCID: PMC4169248.
- Mabb AM, Judson MC, Zylka MJ, Philpot BD. Angelman syndrome: insights into genomic imprinting and neurodevelopmental phenotypes. Trends Neurosci. 2011;34(6):293-303. doi:10.1016/j.tins.2011.04.001. PMID: 21592595; PMCID: PMC3116240.
- McCann KL, Baserga SJ. Long noncoding RNAs as sinks in Prader-Willi syndrome. Mol Cell. 2012;48(2):155-157. doi:10.1016/j.molcel.2012.10.005. PMID: 23102265; PMCID: PMC3496270.
- Polex-Wolf J, Lam BY, Larder R, Tadross J, Rimmington D, Bosch F, et al. Hypothalamic loss of Snord116 recapitulates the hyperphagia of Prader-Willi syndrome. J Clin Invest. 2018;128(3):960-969. doi:10.1172/JCI97007. PMID: 29376887; PMCID: PMC5824864.
- Butler MG, Silvey S, van Bosse HJP. Barriers, limitations, and experiences with clinical trials-treatment in rare diseases with Prader-Willi syndrome as an example. Genes (Basel). 2025;16(12):1436. doi:10.3390/genes16121436. PMID: 41465109; PMCID: PMC12732491.
- Milazzo C, Mientjes EJ, Wallaard I, Rasmussen SV, Erichsen KD, Kakunuri T, et al. Antisense oligonucleotide treatment rescues UBE3A expression and multiple phenotypes of an Angelman syndrome mouse model. JCI Insight. 2021;6(15):e145991. doi:10.1172/jci.insight.145991. PMID: 34369389; PMCID: PMC8410092.
3billion 뉴스레터 구독자만을 위한
희귀질환 진단 최신 정보를 받아보세요.

3billion Inc.
희귀질환 환자들이 진단과 치료에서 외면받지 않는 세상을 만들기 위해 쓰리빌리언은 하나의 미션을 바라봅니다.