hEDS vs vEDS 감별 진단의 핵심: Beighton Score의 한계와 유전자 검사의 역할
단순 유연성인가, 치명적 결합조직 질환인가?
진단의 함정 — “유연한 것”과 “위험한 것”의 경계

관절이 너무 잘 늘어난다며 찾아온 20대 여성 환자 떠올려 보십시오. Beighton Score 7점, 피부 과탄력성, 재발성 탈구 병력까지. 교과서적인 hEDS처럼 보입니다. 하지만 환자의 가족 중 누군가가 원인 불명의 동맥 파열로 사망했다는 사실이 마음에 걸릴 겁니다. 하지만 이 불안을 바로 해소할 방법이 없어 답답하기만 합니다.
이것이 바로 EDS 감별 진단이 단순한 학문적 문제를 넘어 생사를 가르는 임상적 결정이 되는 이유입니다. hEDS(과운동성형)는 가장 흔한 아형이지만, vEDS(혈관형, COL3A1 변이)는 첫 번째 혈관 이벤트가 곧 사망으로 이어질 수 있는 가장 치명적인 아형입니다. 두 질환은 표현형이 겹치고, 현재 우리가 가장 많이 사용하는 스크리닝 도구인 Beighton Score는 이 두 가지를 구분하지 못합니다.
Part 1. Beighton Score, 왜 이것만으로는 부족한가?
Beighton Score는 전신 관절 과유연성(Generalized Joint Hypermobility, GJH)의 대표적인 측정 도구로, 1998년 Brighton 기준과 2017년 국제 분류 기준에서 핵심 지표로 채택되었습니다. 그러나 2023-2025년 최신 연구들은 이 도구의 구조적 한계를 명확히 지적하고 있습니다.
1) 인구통계학적 편향 (Demographic Bias)
2023년 Feldman 등의 리뷰에 따르면, Beighton Score의 컷오프 기준은 연령, 성별, 인종에 따른 표준화가 충분히 이루어지지 않았습니다. 이로 인해 유연성이 높은 소아는 과잉 진단, 반대로 성인 남성이나 특정 인종 집단은 과소 진단될 위험이 실제로 존재합니다. 즉, 점수 자체가 인구 집단에 따라 서로 다른 임상적 의미를 가집니다.
2) 신체 부위의 편향된 선택
현재 기준은 소지 신전, 엄지 굴곡, 팔꿈치 과신전, 무릎 과신전, 체전굴 등 5개 부위만을 평가합니다. 정작 환자들이 가장 아파하는 어깨, 고관절, 척추, 근막과 힘줄은 평가 대상에 없습니다. 환자가 점수가 낮다고 해서 병리적 부담이 낮다는 의미가 아닙니다.
3) 병리 기전과의 구조적 괴리
Beighton Score 점수와 실제 조직 두께 이상 또는 혈류 장애 사이에는 유의미한 상관관계가 없습니다 (Sulli et al., 2023). 이는 점수가 높다고 해서 콜라겐 병리의 심각도를 대변하지 않는다는 것을 의미합니다. 특히 vEDS의 경우, 과유연성이 거의 없는 환자에서도 치명적인 혈관 이벤트가 발생할 수 있습니다.
[도표1] Beighton Score의 한계 요약
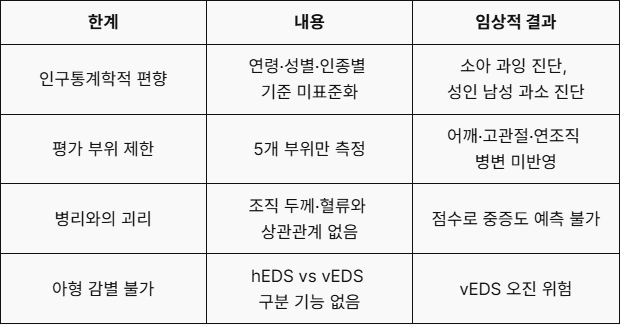
Part 2. hEDS와 vEDS — 겹치는 표현형, 다른 운명
표현형의 연속성이 만드는 함정
hEDS, cEDS, vEDS는 임상 증상이 서로 뚜렷하게 나뉘지 않고 연속적으로 겹칩니다. 같은 가족 내에서도 어떤 구성원은 hEDS로, 다른 구성원은 cEDS로 진단받는 사례가 있을 만큼, 임상 증상만으로 아형을 구분하기는 매우 어렵습니다 (Rahmoune et al., 2023). 이 임상적 중첩이 바로 vEDS를 가장 위험하게 만드는 요소입니다. 의심하지 않으면 검사하지 않고, 검사하지 않으면 진단하지 못합니다.

vEDS의 위험성: COL3A1 변이가 만드는 시한폭탄
vEDS는 COL3A1 유전자 변이로 인해 III형 콜라겐이 결함을 가지며, 이는 혈관 벽과 장 벽의 구조적 취약성으로 직결됩니다. 증상이 경미해 보이거나 심지어 증상이 없는 상태에서도 갑작스러운 동맥 파열 또는 장기 천공이라는 치명적 결과가 발생할 수 있습니다.
Marfan 증후군이나 Loeys-Dietz 증후군 환자들과 비교했을 때, COL3A1 변이 보유자는 말초 동맥 이벤트(박리, 파열 등) 발생률이 20.8%로 가장 높고, 발생 시기도 가장 이릅니다 (Calderón-Martínez et al., 2025). 이 수치는 임상의가 vEDS를 반드시 감별 대상으로 상정해야 한다는 근거입니다.
Part 3. “첫 파열 이전에” — 놓치지 말아야 할 새로운 Red Flags
2017년 국제 분류 기준을 보완하는 최신 근거(2023-2025)는 임상 현장에서 더 일찍 vEDS를 의심할 수 있는 신호를 제시합니다.
가족력이 없는 소아의 설명되지 않는 멍(Easy Bruising)은 유전자 검사 의뢰로 이어지는 가장 흔한 계기입니다. 이는 흔히 혈액 질환으로 먼저 접근하게 되어 진단이 지연되는 경우가 많습니다.
선천성 만곡족(Clubfoot)과 원위부 관절 구축은 고관절 탈구보다 vEDS 환자에게서 더 빈번하게 관찰되는 초기 징후로 보고되었으며, 출생 시부터 결합조직 병리를 의심할 수 있는 단서가 됩니다.
조산 및 양막대 증후군(Amniotic Band Sequence) 역시 vEDS 환자군에서 높은 비율로 관찰되어 새로운 초기 위험 지표로 제안되었습니다 (Bowen et al., 2023).
젊은 층(40세 미만)의 원인 불명 기흉 반복 또는 심한 정맥류는 COL3A1 변이를 적극적으로 의심해야 하는 시나리오입니다 (Sun et al., 2023).
Part 4. 수치로 보는 vEDS의 위협성
“나중에 검사해도 되겠지”라는 생각, 얼마나 위험한지 데이터가 말해줍니다.
유전자 확진을 받은 소아 vEDS 환자의 약 21%(5명 중 1명)는 18세가 되기 전에 이미 동맥 파열 또는 장 천공을 경험합니다. 첫 이벤트 발생 연령의 중앙값은 11세이며, 1세 미만 영아기에도 혈관 이벤트가 발생한 사례가 있습니다 (Wilkinson et al., 2024).
뿐만 아닙니다. 진단되지 않은 14세 소년의 대동맥 파열로 인한 사망 사례도 있습니다. 이 사례는 선제적 진단이 단순한 의료적 권고가 아니라 생존을 결정하는 행위임을 보여줍니다.
Part 5. 유전자 검사 — 병명을 붙이는 것이 아니라, 생존 전략을 수립하는 것
분자 진단이 바꾸는 임상 경로
유전자 검사 결과 한 장이 환자 관리의 모든 것을 바꿉니다.
COL3A1 변이 확인(vEDS 확진) 시, 임상 경로는 즉시 전환됩니다. 평생에 걸친 대동맥 및 중소형 동맥의 정기적 영상 모니터링(CT/MRI)이 즉시 시작되고 (Bowen et al., 2023), 베타차단제, ARB, Celiprolol 등 근거 중심의 예방적 약물 치료가 가능해집니다. 소아기부터 접촉 스포츠, 중량물 취급, 혈압 상승을 유발하는 활동을 제한하여 예기치 못한 파열을 예방하는 라이프스타일 조정도 시작됩니다 (Wilkinson et al., 2024).
hEDS나 다른 아형으로 추정되는 경우, 유전자 검사의 일차적 역할은 hEDS를 ‘확진’하는 것이 아니라, 치명적인 다른 아형(특히 vEDS)을 배제(Rule-out)하는 것입니다 (Doolan et al., 2023). 만약 hEDS로 간주했던 환자가 검사를 통해 다른 유전적 아형(예: THBS2 변이)으로 재분류된다면, 감시 강도를 vEDS 수준으로 높여 환자의 생명을 구할 수 있습니다 (Hadar et al., 2024).
NGS 패널 검사가 단일 유전자 검사보다 나은 이유
Marfan 증후군, Loeys-Dietz 증후군, vEDS 등은 임상 증상이 서로 겹치는 경우가 많습니다. FBN1, COL3A1, TGFBR1/2 등을 포함한 NGS 패널로 한 번에 스크리닝하는 것은 비용 효율적이며 진단율이 높습니다 (Brancato et al., 2025).
또한 NGS 패널은 가족력이 있는 무증상 소아나 친척들에게 예측 검사(Predictive Testing)를 제공하는 유일한 도구입니다. 이는 첫 이벤트가 발생하기 전에 해당 개인을 감시 프로그램에 등록시킬 수 있게 합니다.
Part 6. 고위험 시나리오: 임신과 vEDS
과거에는 vEDS 환자에게 임신을 적극적으로 권장하지 않았습니다. 모성 사망률에 대한 우려 때문이었습니다. 그러나 유전자 확진과 전문 센터 집중 관리가 가능해진 현재, 상황이 달라졌습니다.
유전자 확진 후 전문 센터에서 집중 관리를 받은 121건의 임신 사례에서 치명적인 혈관 이벤트가 발생하지 않았습니다 (Van Den Bersselaar et al., 2025). 이는 유전자 검사가 단순히 위험을 알리는 것을 넘어, 보다 정교하고 개별화된 가족 계획 가이드를 가능하게 한다는 것을 의미합니다.
임신을 계획 중이거나 임신 중인 여성에서 EDS가 의심된다면, 유전자 확진 여부는 단순한 진단적 완결성이 아니라 생존의 문제입니다.
결론: 임상의를 위한 의사결정 프레임워크 제안
EDS의 아형 감별 진단에서 우리가 가져야 할 실용적 접근을 정리하면 다음과 같습니다.
Beighton Score는 여전히 유용한 시작점이지만, 그것으로 ‘확진’과 ‘안심’을 동시에 얻으려 해서는 안 됩니다. 점수가 낮다고 해서 vEDS를 배제할 수 없고, 점수가 높다고 해서 hEDS를 확진할 수 없습니다.
임상 현장에서 다음 시나리오에 해당하는 경우, 유전자 검사를 적극적으로 고려해야 합니다. 어린 나이에 원인 불명의 멍이 반복되는 경우, 가족력 중 동맥 파열이나 갑작스러운 사망이 있는 경우, 40세 미만에서 원인 불명의 기흉이나 장 파열이 발생한 경우, 임신을 앞두고 있는 EDS 의심 환자, 그리고 임상 증상으로 아형 결정이 모호한 모든 케이스입니다.
분자 진단은 단순히 병명을 붙이는 행위가 아닙니다. vEDS를 조기에 확인하여 영상 모니터링을 시작하고, 예방적 치료를 적용하며, 환자와 가족 전체의 위험을 구조화된 방식으로 관리하는 것이 유전자 검사가 제공하는 실질적인 임상 가치입니다.
“첫 번째 파열 이전에 진단하라.” 이것이 2026년 EDS 임상 관리의 핵심 명제입니다.
임상 소견만으로 아형 감별이 어려운 경우, 유전자 검사는 결정적인 근거를 제공합니다.
검사 적합성, 해석 전략에 대해 전문 상담원과 상의해 보십시오.
참고 문헌 및 DOI
- Aziz Q, et al. (2025). Clinical Practice Updates: AGA Clinical Practice Update on GI Manifestations and Autonomic or Immune Dysfunction in Hypermobile Ehlers-Danlos Syndrome: Expert Review. https://doi.org/10.1016/j.cgh.2025.02.015
- Bowen JM, et al. (2023). Diagnosis and management of vascular Ehlers-Danlos syndrome: Experience of the UK national diagnostic service, Sheffield. https://doi.org/10.1038/s41431-023-01343-7
- Brancato V, et al. (2025). NGS Approaches in Clinical Diagnostics: From Workflow to Disease-Specific Applications. https://doi.org/10.3390/ijms26199597
- Calderón-Martínez E, et al. (2025). Differences in Arterial Events in Vascular Ehlers-Danlos, Loeys-Dietz, and Marfan Syndrome. https://doi.org/10.1016/j.jacc.2025.04.023
- Doolan BJ, et al. (2023). Dermatologic manifestations and diagnostic assessments of the Ehlers-Danlos syndromes: A clinical review. https://doi.org/10.1016/j.jaad.2023.01.034
- Feldman EM, et al. (2023). A narrative review of the literature on illness uncertainty in hypermobile ehlers-danlos syndrome. https://doi.org/10.1186/s12969-023-00908-6
- Hadar N, et al. (2024). Heterozygous THBS2 pathogenic variant causes Ehlers–Danlos syndrome with prominent vascular features in humans and mice. https://doi.org/10.1038/s41431-024-01559-1
- Haem E, et al. (2025). Vascular Ehlers-Danlos Syndrome and Pregnancy: A Systematic Review. https://doi.org/10.1097/01.aoa.0001125536.76136.aa
- Rahmoune H, et al. (2023). The Ehlers-Danlos syndrome, a disease of late diagnosis: report two cases. https://doi.org/10.1093/rheumatology/kead323.054
- Sulli A, et al. (2023). NAILFOLD CAPILLAROSCOPIC STATUS IN HYPERMOBILE EHLERS DANLOS SYNDROME PATIENTS: PILOT INVESTIGATION. https://doi.org/10.1136/annrheumdis-2023-eular.4886
- Sun Y, et al. (2023). Case report of a young male, with recurrent pneumothorax, hemoptysis and intrapulmonary cavitary lesions. https://doi.org/10.1097/md.0000000000035436
- Van Den Bersselaar LR, et al. (2025). Pregnancy and Delivery Outcomes in Vascular Ehlers–Danlos Syndrome: A Retrospective Multicentre Cohort Study. https://doi.org/10.1111/1471-0528.18142
- Wang J, et al. (2025). Fascial Pathophysiology in Hypermobility Spectrum Disorders and Hypermobile Ehlers–Danlos Syndrome: A Review of Emerging Evidence. https://doi.org/10.3390/ijms26125587
- Wilkinson JM, et al. (2024). Vascular Ehlers-Danlos syndrome in children: evaluating the importance of diagnosis and follow-up during childhood. https://doi.org/10.1038/s41431-024-01773-x
3billion 뉴스레터 구독자만을 위한
희귀질환 진단 최신 정보를 받아보세요.

3billion Inc.
희귀질환 환자들이 진단과 치료에서 외면받지 않는 세상을 만들기 위해 쓰리빌리언은 하나의 미션을 바라봅니다.





